近日,Plant Biotechnology Journal杂志在线发表了实验室傅竞也/王强研究团队完成的题为“ZmWRKY29 Transcriptionally Represses ZmRBOHC to Attenuate ROS Production and Facilitates Gibberella Stalk Rot Susceptibility in Maize”的研究论文。该研究鉴定到受禾谷镰孢菌侵染诱导表达的转录抑制因子ZmWRKY29,系统阐明了其通过直接抑制ZmRBOHA/ZmRBOHC的转录,减少活性氧(ROS)的产生进而削弱玉米对禾谷镰孢茎腐病(Gibberella Stalk Rot,GSR)抗性的机制,为玉米抗病育种提供了潜在的靶点。

茎腐病(Stalk rot)是玉米生产上极具毁灭性的茎部病害,主要发生在生殖生长阶段的抽雄吐丝期。受侵染玉米植株的水分与养分吸收能力严重受损,极易发生倒伏,最终造成大幅减产。茎腐病病原包括镰孢菌与腐霉菌,其中禾谷镰孢菌(Fusarium graminearum,有性态为 Gibberella Zeae)为主要病原。但目前仅有少量抗性QTL与抗病基因被鉴定参与调控禾谷镰孢茎腐病(GSR)的抗性,感病基因更鲜少报道,可被利用的基因资源仍十分匮乏。
1. ZmWRKY29是一个受禾谷镰孢菌侵染诱导标的的转录抑制因子
作者前期研究发现ZmWRKY29的表达与萜类植保素合成基因有较高相关性,均响应禾谷镰孢菌的侵染,但其并不调控萜类植保素合成基因的表达,暗示其在玉米与禾谷镰孢菌互作中发挥其他功能。表达分析发现,在禾谷镰孢菌侵染1h后,ZmWRKY29的表达即被快速诱导,水杨酸(SA)与茉莉酸(JA)的处理同样能够显著激活ZmWRKY29的表达(图1A-C)。亚细胞定位表明,ZmWRKY29定位于细胞核(图1D)。利用酵母GAL4报告系统与原生质体的报告系统发现ZmWRKY29具有转录抑制活性(图1E,1F)。
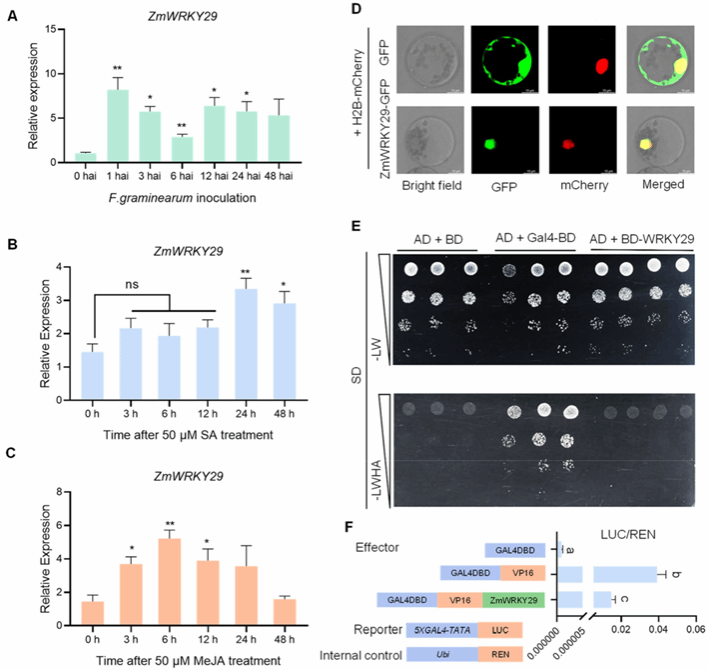
图1. ZmWRKY29被禾谷镰孢菌侵染诱导表达且具有转录抑制活性
2.过表达ZmWRKY29增强玉米对禾谷镰孢菌的感病性
为了探究ZmWRKY29在玉米与禾谷镰孢菌互作中的功能,作者创制了该基因的两个独立过表达系(#59, #83),ZmWRKY29在过表达系中的表达水平显著高于野生型(图2A)。对玉米幼苗茎部接种禾谷镰孢菌菌丝 4 天后,过表达株系的病斑长度较野生型显著增加(图2B, 2C),相对真菌生物量也大幅升高 (图2D)。根系也是禾谷镰孢菌侵染宿主的重要部位,在对根系进行抗病性鉴定后发现,过表达 ZmWRKY29 同样增加了根系发病程度,真菌生物量也显著升高(图2E-2G)。进一步对成熟的玉米茎部接种禾谷镰孢菌孢子,7 天后观察发现,过表达株茎内褐色腐烂病斑长度显著长于野生型(图2I)。以上结果表明ZmWRKY29是玉米GSR的负调控因子。
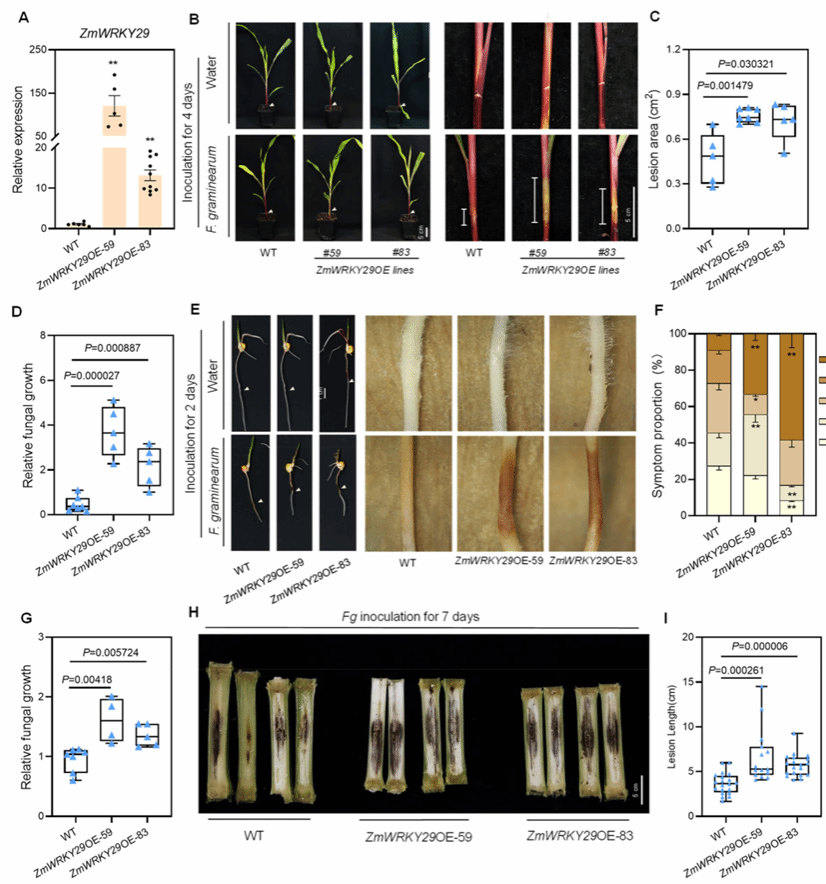
图2. 过表达ZmWRKY29降低玉米对禾谷镰孢菌的抗性
3.过表达ZmWRKY29减少活性氧的产生与胼胝质的沉积
活性氧(ROS)的产生是植物应对病原菌侵染的常见反应,对宿主免疫至关重要。为探究ZmWRKY29是否影响禾谷镰孢菌侵染下的 ROS 生成,作者首先对受侵染茎秆进行 DAB 染色,结果显示与野生型(WT)相比,ZmWRKY29过表达株系的红棕色更浅、菌丝更多,说明其 ROS 积累更少,真菌入侵与增殖更为严重(图 3A)。H₂O₂含量检测进一步证实,ZmWRKY29过表达株系的 ROS 的含量较野生型更低(图 3B)。此外,几丁质诱导的ROS 爆发也在ZmWRKY29过表达株系中显著减弱(图 3C)。胼胝质沉积也是植物响应生物胁迫的重要特征。如图 3D、3E 所示,野生型受侵染茎秆的胼胝质沉积显著高于ZmWRKY29过表达株系。综上所述,ZmWRKY29过表达会降低 ROS 生成与胼胝质沉积,这可能是其对禾谷镰孢菌敏感性增强的原因。
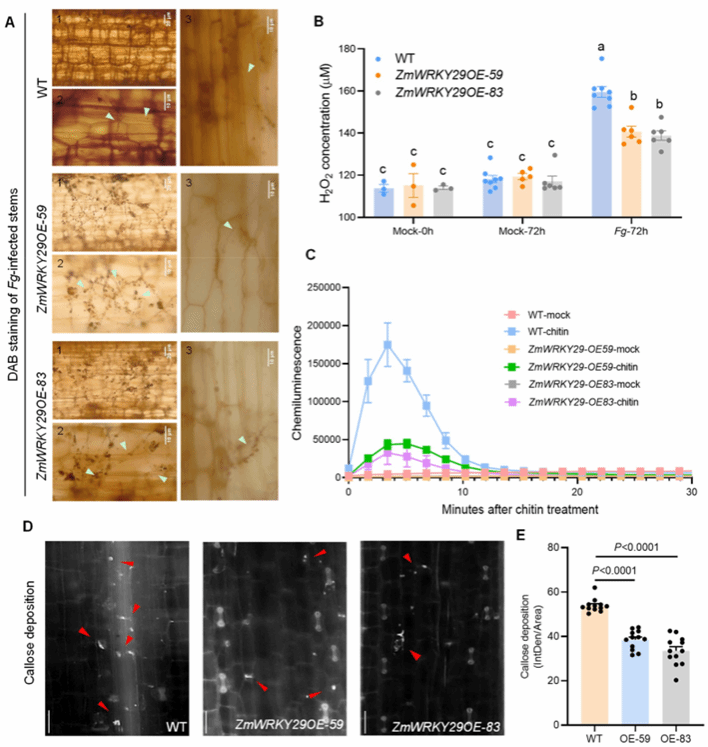
图3. ZmWRKY29过表达削弱禾谷镰孢菌侵染下ROS的产生与胼胝质的沉积
4. ZmWRKY29的突变增强ROS的积累并提高GSR的抗性
为了进一步验证ZmWRKY29在GSR抗性中的功能,作者在ChinaMu突变体库中获得了ZmWRKY29的 Mu 转座子插入突变体(图4A)。苗期茎秆接种结果显示,Zmwrky29-mu对 GSR 抗性显著增强,病斑长度与病原菌生物量显著降低(图4B-4D);成熟期田间接种结果同样发现Zmwrky29-mu突变体病斑长度显著短于野生型(图4E, 4F)。除此之外,Zmwrky29-mu中几丁质诱导的 ROS 爆发强度也显著高于野生型(图4G);DAB 染色显示突变体产生更多棕褐色沉淀(图4H);H2O2 含量检测进一步证实Zmwrky29-mu突变中体ROS 积累显著增加(图4I)。综上所述,ZmWRKY29能够抑制ROS的产生,是玉米GSR抗性的负调控因子。
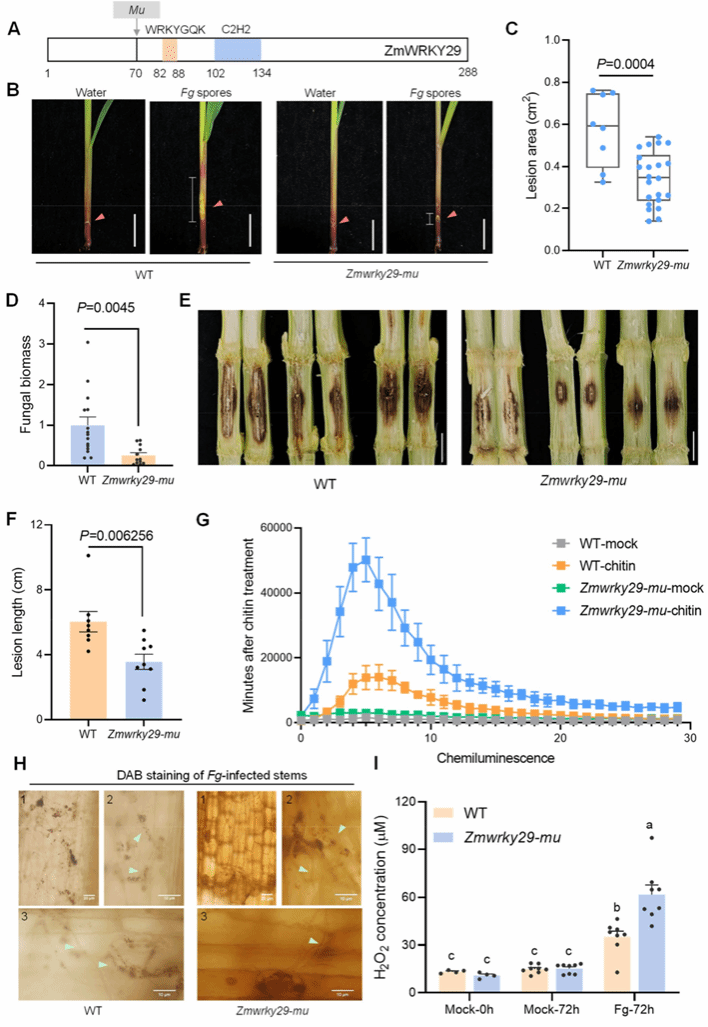
图4. ZmWRKY29的突变增强玉米GSR抗性与ROS的产生
5. ZmWRKY29抑制ZmRBOHA与ZmRBOHC的表达
为解析ZmWRKY29调控GSR抗性与ROS产生的机制,该研究对野生型和ZmWRKY29过表达植株在接种 0 h 和 24 h 后进行RNA-seq分析。RBOH是病原菌诱导 ROS 产生的关键酶,作者在差异表达基因中筛选到ZmRBOHA和ZmRBOHC,二者在过表达材料中的表达较野生型更低(图5A-5C)。通过双荧光素酶报告系统,作者发现ZmWRKY29 可显著抑制ZmRBOHA和ZmRBOHC的启动子活性(图5D-F)。WRKY 转录因子通常结合靶基因启动子的 W‑box 元件。作者对启动子进行系列缺失与点突变,结果显示:即使突变 ZmRBOHA 启动子最后一个 W‑box,ZmWRKY29 仍能抑制其转录活性(图5G),说明ZmWRKY29对ZmRBOHA的调控可能还依赖其他元件获其他因子;而当ZmRBOHC 启动子中 -128 bp 处的 W‑box 突变后,ZmWRKY29对其抑制作用消失,表明该位点是 ZmWRKY29 的关键作用位点(图5H)。
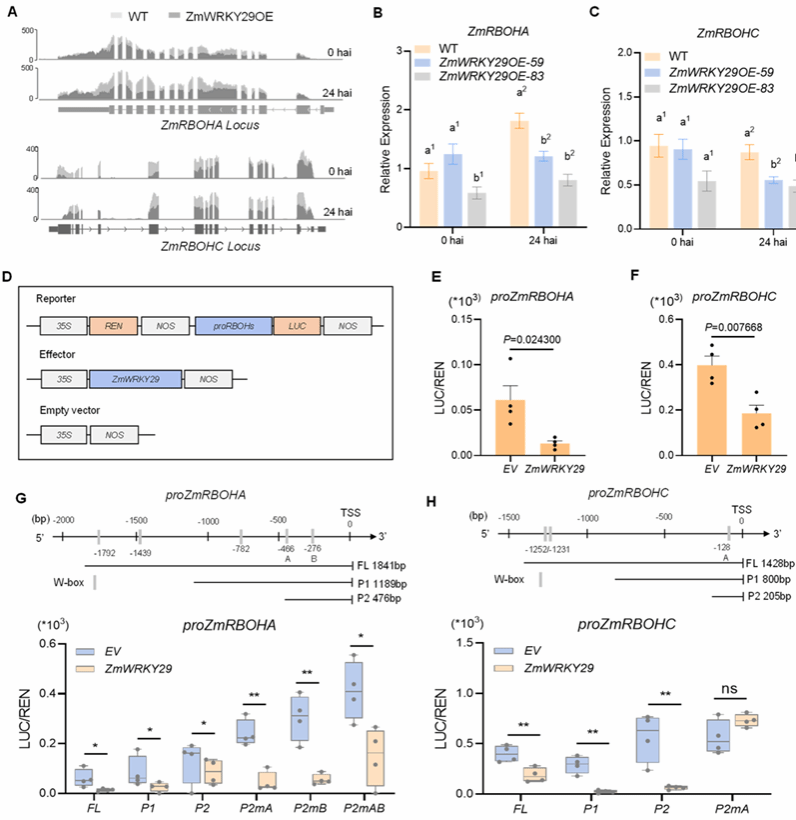
图5. ZmWRKY29负调控ZmRBOHA与ZmRBOHC的表达
进一步的DAP‑qPCR 实验显示,ZmWRKY29 可直接结合 ZmRBOHA 启动子上多个含 W‑box 的区域(图6A);对富集度最高的 -468 bp 区域进行 EMSA 实验,证实其在体外可直接结合该片段(图6B)。烟草叶片中的 DLR 实验进一步验证了 ZmWRKY29 对 ZmRBOHA 启动子的抑制作用(图6C)。同样,DAP‑qPCR 显示 ZmRBOHC 启动子 -128 bp 含 W‑box 的区域被ZmWRKY29显著富集(图6D);酵母单杂交(Y1H)与 EMSA 均证实 ZmWRKY29 直接结合该位点,烟草 DLR 实验也验证了这一抑制效果(图6E-G)。综上所述,ZmWRKY29 可直接结合 ZmRBOHA 和 ZmRBOHC 的启动子并抑制其转录,其中对 ZmRBOHA 的抑制可能还依赖其他因子。
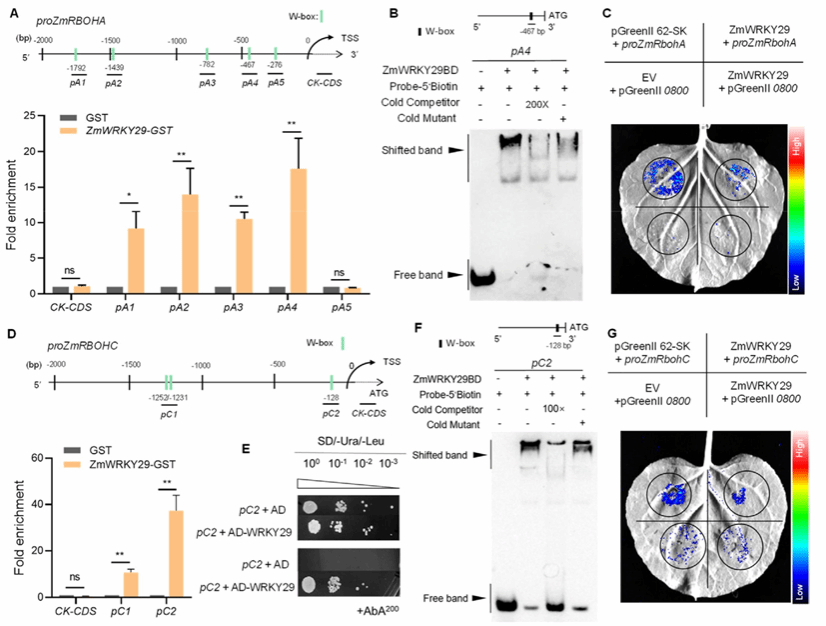
图6. ZmWRKY29直接结合ZmRBOHA与ZmRBOHC的启动子
6. ZmRBOHC正调控玉米对GSR的抗性
为了明确ZmWRKY29 靶向抑制的 ZmRBOHC 是否调控玉米对GSR的抗性,作者获得了EMS 诱变的 zmrbohc 突变体,该突变体在1152 bp处发生C/A 单碱基替换,导致蛋白在第384 位氨基酸出现提前终止(图7A)。随后,作者对幼苗茎部接种禾谷镰孢菌菌丝。结果显示,zmrbohc 突变体的发病症状显著加重,病斑面积与长度均显著扩大(图7B-7D)。同时,在成株期对玉米茎秆进行田间接种也得到了相似结果(图7E, 7F)。除了GSR抗性显著下降外,zmrbohc 突变体中几丁质诱导的 ROS 爆发也明显减弱(图7G)。以上结果表明,ZmRBOHC 是玉米GSR抗性的正调控因子。禾谷镰孢菌可通过招募 ZmWRKY29 靶向并抑制 ZmRBOHC 的转录,进而减少 ROS 产生,最终导致感寄主病。
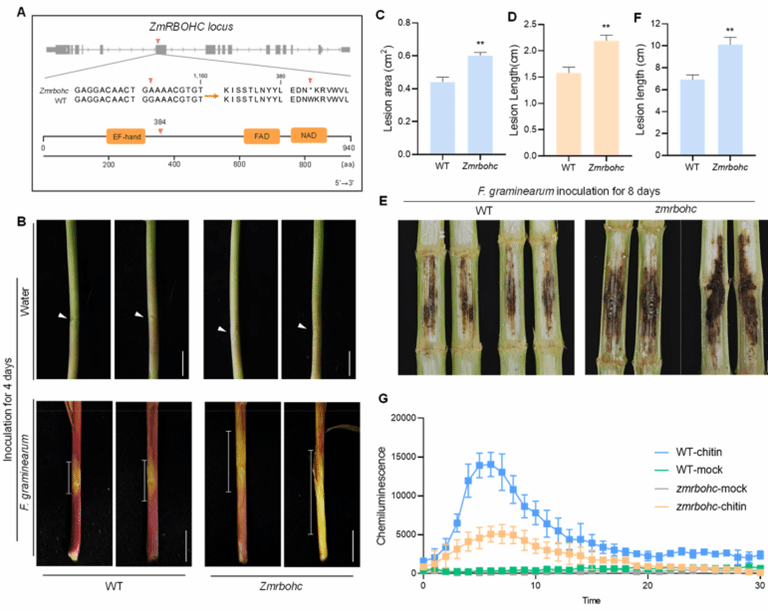
图7. Zmrbohc突变体对GSR抗性降低
综上,该研究发现,在禾谷镰孢菌侵染下,ZmWRKY29 的表达被快速诱导,随后,ZmWRKY29 直接结合 ZmRBOHC 启动子区域的 W‑box 元件,抑制其转录,进而降低 ZmRBOHC 介导的活性氧(ROS)产生,最终削弱玉米对GSR的抗性,促进禾谷镰孢菌的侵染(图8)。
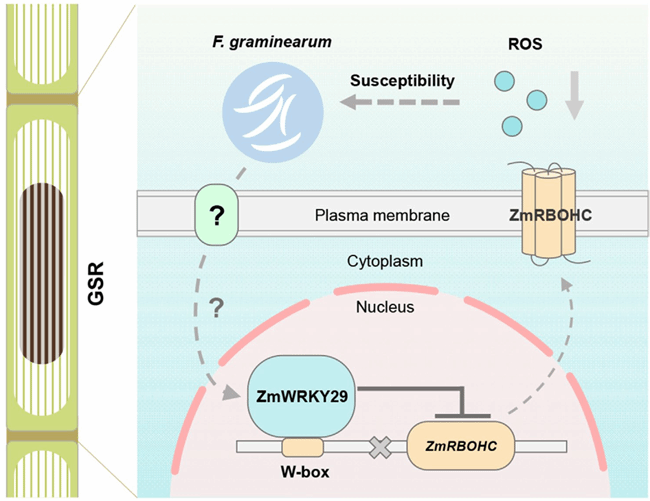
图8. ZmWRKY29负调控玉米GSR抗性的机制模式图
实验室傅竞也讲师与已毕业硕士研究生朱丽为该论文的共同第一作者,傅竞也讲师与王强教授为该论文的共同通讯作者。该研究得到了国家自然科学基金(32001446)与四川省自然科学基金(2024NSFSC0332)的资助。
原文链接:https://doi.org/10.1111/pbi.70629