在自然界中,植物持续面临病原菌的包围与侵袭。然而,植物的免疫系统却常常陷入两难——既要迅速调动力量击退入侵者,又必须避免“杀敌一千,自损八百”的过度反应。一旦免疫应答失控,植物不仅会因细胞损伤和能量过度消耗而受损,生长发育也将受到严重抑制。因此,在成功抵御病原菌之后,如何及时为免疫系统“踩下刹车”、恢复体内平衡,成为植物适应环境、确保生存繁衍的关键技能。然而,长期以来,调控这一过程的分子机制一直是未解之谜。
近日,实验室陈学伟教授团队在国际知名学术期刊Science Bulletin(IF=21.1)上在线发表了题为《A phospho-switch centered on OsAHL23 orchestrates immune homeostasis in rice》(以OsAHL23为核心的磷酸化开关协调水稻免疫稳态)的研究成果。该研究揭示了一个由激酶OsMPK5、磷酸酶PP2A-A和转录因子OsAHL23构成的调控回路。该回路通过精准控制OsAHL23第321位丝氨酸(S321)的可逆磷酸化形成的“分子开关”,动态平衡水稻的免疫反应与生长发育。
AHL家族转录因子在植物中广泛存在,参与多种生理过程的调控,但该家族在水稻中的具体功能一直未得到充分解析。该研究发现,当稻瘟菌来袭时,水稻的OsAHL23基因会被迅速激活,尤其在叶片(稻瘟病最常发生的部位)表达量显著上升。进一步实验显示,敲除OsAHL23基因后,水稻对稻瘟病的抗性显著增强,但伴随着产量下降;反过来,OsAHL23过量表达虽然提升产量,却增加感病风险。机制解析表明,OsAHL23蛋白通过促使OsNTL6抑制防御基因OsWRKY45和OsPR1b的表达,起到给免疫系统“踩刹车”的作用。
这个“刹车”系统本身还受一个精细调控开关的控制,即OsAHL23蛋白S321位点的可逆磷酸化。具体而言,稻瘟菌侵染时,磷酸酶PP2A-A积累并特异性去磷酸化OsAHL23的S321位点,导致其转录活性降低,从而解除对免疫反应的抑制,水稻进入“战斗状态”;在击退病原菌后,PP2A-A蛋白水平下降,激酶OsMPK5重新对OsAHL23的S321位点进行磷酸化修饰,恢复其活性,使免疫系统再度回归“刹车”。这一可逆的“磷酸化开关”正是水稻实现免疫平衡精准调控的分子基础。
值得注意的是,这套“磷酸化开关”系统在玉米、番茄等不同植物中高度保守,提示这一机制可能是植物界进化上保守的免疫稳态调控策略。该研究不仅系统解析了水稻如何协调抗病与高产平衡的科学问题,也为作物抗病与高产协同改良提供了新的理论依据和分子靶点。未来通过精准调控这一“开关”,有望培育兼具广谱抗病性与高产的作物新品种。
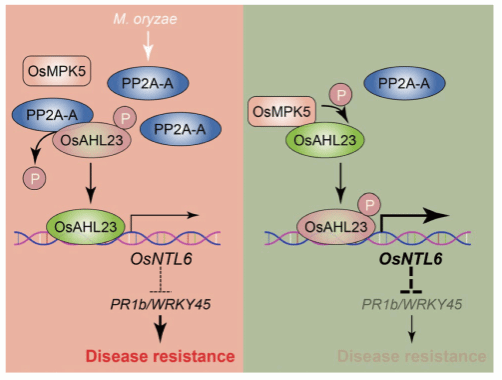
图1 PP2A-A和OsMPK5调控OsAHL23磷酸化开关维持水稻免疫平衡的模式图
实验室博士研究生马招堂、已毕业硕士研究生何琦、已毕业的博士生廖海澄(现四川农业大学副教授)为论文共同第一作者,陈学伟教授和廖海澄副教授为共同通讯作者。该研究得到了国家重点研发计划、国家自然科学基金、四川省自然科学基金、新基石科学基金会科学探索奖和新基石研究员项目等项目的资助。
文章链接:https://www.sciencedirect.com/science/article/pii/S2095927326002471